"Molekul Polar" dan "nonpolar" redirect di sini. Untuk kegunaan lain dari istilah "Polar", lihat Polar .

Sebuah molekul air , contoh yang sering digunakan dari polaritas. Kedua tuduhan hadir dengan muatan negatif di tengah (warna merah), dan muatan positif di ujung (warna biru).
Teori
Elektron tidak selalu dibagi rata antara dua atom ikatan, satu atom mungkin mengerahkan kekuatan lebih pada awan elektron daripada yang lain. Ini "tarik" disebut elektronegativitas dan mengukur daya tarik untuk elektron sebuah atom tertentu memiliki. Pembagian yang tidak merata elektron dalam sebuah ikatan mengarah pada pembentukan listrik dipol : pemisahan muatan listrik positif dan negatif. Biaya parsial dilambangkan sebagai δ + ( delta plus) dan δ-(delta minus). Simbol-simbol ini diperkenalkan oleh Christopher Ingold dan istrinya Hilda Usherwood pada 1926. [1]Atom dengan elektronegativitas tinggi - seperti fluor , oksigen , dan nitrogen - mengerahkan tarik lebih besar pada elektron dari atom yang memiliki elektronegativitas yang lebih rendah. Dalam obligasi, hal ini dapat menyebabkan pembagian yang tidak merata elektron antara atom, sebagai elektron akan bergerak mendekat pada atom dengan elektronegativitas yang lebih tinggi.
Obligasi dapat jatuh antara satu dari dua ekstrem - yang benar-benar nonpolar atau benar-benar polar. Ikatan sepenuhnya nonpolar terjadi ketika elektronegativitas adalah identik dan karenanya memiliki perbedaan dari nol. Sebuah ikatan sepenuhnya kutub lebih tepat disebut ikatan ion dan terjadi ketika perbedaan antara elektronegativitas cukup besar sehingga satu atom mengambil elektron dari yang lain. Obligasi Istilah "kutub" dan "nonpolar" biasanya mengacu pada ikatan kovalen . Untuk menentukan polaritas ikatan kovalen menggunakan cara numerik, perbedaan elektronegativitas antara atom-atom diambil. Jika hasilnya adalah antara 0,4 dan 1,7 kemudian, umum, obligasi adalah polar kovalen.
Polaritas molekul
Sedangkan molekul dapat digambarkan sebagai "kovalen polar", "nonpolar kovalen", atau "ion", ini sering merupakan istilah relatif, dengan satu molekul sederhana menjadi lebih polar atau lebih nonpolar daripada yang lain. Namun, sifat berikut ini khas molekul tersebut.Sebuah molekul terdiri dari satu atau lebih ikatan kimia antara orbital molekul dari atom yang berbeda. Molekul A mungkin kutub baik sebagai akibat dari ikatan polar karena perbedaan elektronegativitas seperti dijelaskan di atas, atau sebagai akibat dari pengaturan asimetris ikatan kovalen nonpolar dan non-ikatan pasangan elektron dikenal sebagai penuh orbital molekul .
molekul Polar
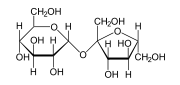
Contoh molekul polar rumah tangga biasa termasuk gula, misalnya sukrosa berbagai gula. Gula memiliki hidrogen oksigen banyak kutub (-OH) kelompok dan secara keseluruhan sangat polar.Karena sifat polar dari molekul air ( H 2 O ) itu sendiri, molekul polar umumnya dapat larut dalam air.
- Contoh 1. The hidrogen fluorida , HF, molekul polar yang berdasarkan ikatan kovalen polar - dalam elektron ikatan kovalen yang mengungsi ke arah atom fluor lebih elektronegatif.
- Contoh 2. Dalam amonia , NH 3, molekul tiga N-H obligasi hanya memiliki polaritas sedikit (ke arah atom yang lebih elektronegatif nitrogen). Namun, molekul memiliki dua elektron tunggal dalam orbital, yang menunjuk ke arah puncak keempat dari tetrahedron perkiraan, ( VSEPR ). Ini orbital tidak berpartisipasi dalam ikatan kovalen, itu adalah elektron kaya, yang menghasilkan dipol yang kuat di seluruh molekul amonia keseluruhan.
- Contoh 2.5. Dalam ozon , O 3, dua molekul O-O obligasi yang nonpolar (tidak ada perbedaan elektronegativitas antara atom-atom dari unsur yang sama). Namun, distribusi elektron lain tidak merata - karena atom pusat harus berbagi elektron dengan dua atom lain, tetapi masing-masing atom terluar harus berbagi elektron dengan hanya satu atom lain, atom pusat lebih kehilangan elektron daripada yang lain (atom pusat memiliki muatan resmi dari +1, sedangkan atom terluar masing-masing memiliki muatan formal -1 / 2). Karena molekul memiliki geometri membungkuk, hasilnya adalah dipol seluruh molekul ozon secara keseluruhan.
- Hidrogen fluorida : semakin elektronegatif atom fluoride ditunjukkan dengan warna kuning
- Amoniak : dua elektron tunggal yang ditampilkan dalam warna kuning, atom hidrogen dalam putih
molekul nonpolar

Diagram yang menunjukkan efek bersih dari obligasi kutub simetris (arah panah kuning menunjukkan migrasi elektron) di dalam boron trifluorida membatalkan keluar untuk memberikan polaritas bersih dari nol. δ-menunjukkan peningkatan muatan negatif dan + δ menunjukkan peningkatan muatan positif.
Contoh-contoh senyawa nonpolar rumah tangga termasuk lemak, minyak, dan bensin / bensin. Oleh karena itu (per aturan "minyak dan air" ibu jari), molekul yang paling nonpolar yang tidak larut air ( hidrofobik ) pada suhu kamar. Namun, banyak nonpolar pelarut organik , seperti terpentin , mampu melarutkan zat polar. Ketika membandingkan molekul polar dan nonpolar dengan massa molar yang sama, molekul polar pada umumnya memiliki titik didih yang lebih tinggi, karena interaksi dipol-dipol antara molekul mereka. Bentuk yang paling umum seperti interaksi adalah ikatan hidrogen , yang juga dikenal sebagai ikatan H-.
- Contoh 3. Dalam metana molekul (CH 4) empat C-H obligasi diatur tetrahedral di sekitar atom karbon. Setiap obligasi memiliki polaritas (meskipun tidak sangat kuat). Namun, obligasi diatur simetris sehingga tidak ada keseluruhan dipol dalam molekul.
- Contoh 4. The boron trifluorida molekul (BF 3) memiliki susunan planar trigonal dari tiga ikatan polar pada 120 °. Hal ini mengakibatkan tidak keseluruhan dipol dalam molekul.
- Contoh 5. The oksigen molekul (O 2) tidak memiliki polaritas dalam ikatan kovalen karena elektronegativitas yang sama, maka tidak ada polaritas dalam molekul.
- Methane : obligasi yang diatur simetris sehingga tidak ada dipol keseluruhan
- Boron trifluorida : susunan planar trigonal dari tiga hasil obligasi kutub di no dipol keseluruhan
Hibrida
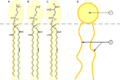
Molekul besar yang memiliki salah satu ujungnya dengan gugus polar terpasang dan ujung lain dengan kelompok nonpolar baik surfaktan . Mereka dapat membantu dalam pembentukan emulsi stabil, atau campuran, air dan lemak. Surfaktan mengurangi tegangan antarmuka antara minyak dan air dengan menyerap pada antarmuka cair-cair.- Molekul kompleks memiliki gugus polar beberapa ( hidrofilik , air-mencintai) di sisi kanan dan rantai nonpolar yang panjang ( lipofilik , lemak-loving) di sisi kiri. Hal ini memberikan surfaktan properti
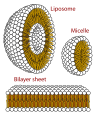
- Sebuah misel - yang lipofilik ujung dari molekul surfaktan larut dalam minyak, sedangkan hidrofilik berakhir dibebankan tetap berada di luar dalam fase air, melindungi sisa hidrofobik micelle. Dengan cara ini, tetesan minyak kecil menjadi larut dalam air.
- Fosfolipid merupakan surfaktan alami yang efektif yang memiliki fungsi biologis yang penting
- Lintas melihat bagian struktur yang dapat dibentuk oleh fosfolipid . Mereka dapat membentuk misel dan merupakan penting dalam membentuk membran sel
polaritas molekul Memprediksi
- Ini tabel klasifikasi memberikan pemahaman umum baik memprediksi dipol molekul dari beberapa struktur molekul umum. Namun, orang tidak boleh menafsirkan secara harfiah:
| Rumus | Deskripsi | Contoh | |
| Polar | AB | Linear Molekul | CO |
|---|---|---|---|
| HA x | Molekul dengan H tunggal | HF | |
| A x OH | Molekul dengan OH di salah satu ujung | C 2 H 5 OH | |
| O x A y | Molekul dengan O di salah satu ujung | H 2 O | |
| N x A y | Molekul dengan N di salah satu ujung | NH 3 | |
| Nonpolar | A 2 | Diatomik molekul dari unsur yang sama | O 2 |
| C x A y | Sebagian besar senyawa karbon | CO 2 |
- Menentukan grup jalur adalah cara yang berguna untuk memprediksi polaritas molekul. Secara umum, molekul tidak akan memiliki momen dipol, jika momen dipol ikatan individu molekul membatalkan satu sama lain. Hal ini karena momen dipol adalah vektor euclidean jumlah dengan besaran dan arah, dan dua vektor yang sama yang saling bertentangan akan membatalkan.
Sejak C 1, C s, C ∞ h C n dan C nv grup jalur tidak memiliki pusat inversi, pesawat cermin horisontal atau beberapa C n axis, molekul dalam salah satu grup jalur akan memiliki momen dipol.














0 komentar:
Posting Komentar